Сотрудники Иркутского института химии им. А. Е. Фаворского СО РАН и Иркутского государственного аграрного университета им. А. А. Ежевского на основе наночастиц селена и каррагинана (высокодоступного полисахарида водорослей) создали нанокомпозиты, способные защищать клетки печени при свободнорадикальных поражениях, сопровождающих различные отравления, токсические и вирусные гепатиты и многие другие болезни. Результаты исследования опубликованы в Colloids and Surfaces B: Biointerfaces. Кроме того, оказалось, что созданные наночастицы обладают удобной для диагностики инфракрасной люминесценцией.
«В биомедицине есть проблема поражения всех живых клеток и особенно клеток печени — гепатоцитов — свободными радикалами. Последние возникают в организме при проникающей радиации, практически всех отравлениях, а также гепатитах, других заболеваниях и вызывают деструкцию клеточных мембран. С высокой долей вероятности это приводит к циррозу печени. Если же свободные радикалы и образующиеся под их действием продукты перекисного окисления липидов мембран поражают органеллы и ядро клетки, то нарушается сам ее генетический код. Она начинает воспроизводиться дефектно (это чревато высоким риском развития рака печени) или вовсе теряет способность к делению (это также приводит к циррозу). В некоторых случаях, например, при очень сильном отравлении, свободных радикалов становится слишком много. Тогда развивается острый токсический гепатит с одновременным поражением всех структурных компонентов гепатоцитов, который, как правило, приводит к неотвратимой и быстрой смерти. Поэтому вопрос, как защитить гепатоциты от атак свободных радикалов, в биомедицине стоит очень остро», — рассказывает заведующий лабораторией функциональных наноматериалов ИрИХ СО РАН Борис Геннадьевич Сухов.
Сейчас для антирадикальной защиты печени используют так называемые антиоксиданты — специальные молекулярные ловушки, которые перехватывают радикалы и не дают им достичь мембраны, органелл и ядра гепатоцитов. Таких антиоксидантов достаточно много, однако они действуют системно — распределяются кровотоком по всему организму, иногда оказывая разнообразные побочные эффекты на отдельные органы и системы. Кроме того, из-за такого распределения в печени оказывается очень малая концентрация необходимых для ее защиты веществ. Гораздо эффективней было бы создать антиоксидант, который привязывался бы исключительно к клеткам печени. Кроме того, важно сделать так, чтобы он имел локальное пролонгированное действие непосредственно на гепатоцитах. Именно такую задачу поставили перед собой ученые ИрИХ СО РАН. Исследование проводилось в рамках молодежного гранта Российского научного фонда («Разработка новых низкодозных антиоксидантных гепатопротекторных препаратов наноселена с целевой доставкой к клеткам печени и пролонгированным действием») под руководством старшего научного сотрудника лаборатории функциональных наноматериалов ИрИХ СО РАН кандидата химических наук Марины Владимировны Лесничей.
«Оказалось, что для использования в качестве антиоксидантов как нельзя кстати подходят наночастицы селена. В зависимости от своего размера каждая из них состоит из тысяч и десятков тысяч атомов. Под действием свободных радикалов связь атомов селен-селен внутри наночастицы легко разрывается, и тогда каждый из них становится способным перехватывать по радикалу. Выполнив свою работу, наночастица селена уменьшается всего на два атома, однако в ней остаются десятки тысяч других, способных снова и снова перехватывать атаки свободных радикалов. Это главное отличие наночастиц селена от молекулярных антиоксидантов, где одна молекула вещества может перехватывать только один радикал», — отмечает Борис Сухов.
Следующий шаг — доставить и привязать синтезированную наночастицу селена к клеткам печени. В качестве оболочки для выполнения этих функций ученые выбрали полисахарид каррагинан. Его галактозные фрагменты специфичны к рецепторам на поверхности гепатоцитов. Галактозосодержащие полисахариды способны связываться с клетками печени и удерживаться на них, более того — проникать через мембрану и попадать внутрь клетки. Кроме того, каррагинан дешев (поскольку в больших количествах добывается из красных морских водорослей), безвреден для организма и уже давно широкомасштабно используется при производстве пищевых продуктов.
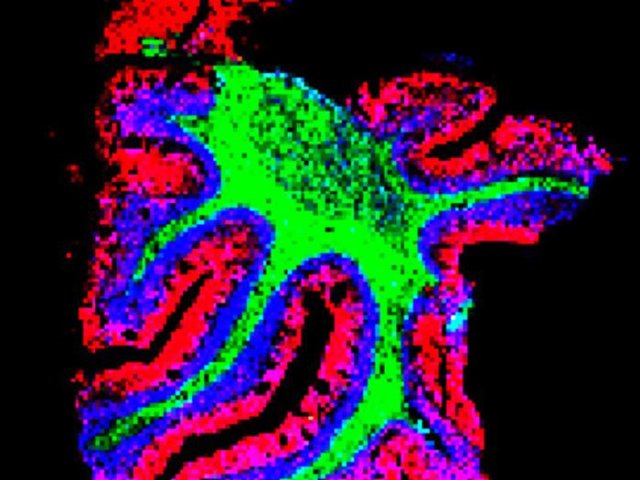
Антирадикальное действие наночастиц селена в полисахаридной каррагинановой оболочке исследователи проверили на модели токсического гепатита у мышей. Для этого с помощью четыреххлористого углерода у животных был смоделирован окислительный стресс (соответствующий тому, что происходит с организмом при отравлении многими токсинами, в том числе алкоголем, этиленгликолем и угарным газом). На первом этапе изучалось профилактическое действие препарата. То есть сначала мышам из экспериментальной группы вводился селеновый нанокомпозит, а уже после — смертельная доза четыреххлористого углерода. Животные из контрольной группы подвергались только воздействию токсина. В результате последние погибли от острого отравления, а большая часть мышей, которым был введен защитный наноселеновый препарат, выжили. «У них произошла достаточно мощная гепатозащита, то есть предполагаемый нами перехват радикалов, который предотвратил развитие смертельных поражений. Это также подтверждается и микроскопическими патоморфологическими исследованиями клеточных тканей печени, — рассказывает Борис Сухов. — Такую особенность препарата потенциально можно применять, чтобы вводить его пожарным перед тем, как они выезжают на вызов. Это позволит избежать отравления угарным газом и другими высокотоксичными продуктами горения. То же самое относится и к профилактике осложнений от предполагаемого воздействия иных токсических веществ, проникающей радиации, а также к защите печени от свободных радикалов, образующихся при инфекционных гепатитах и других заболеваниях».
Затем ученые исследовали терапевтическое действие селенового нанокомпозита на основе каррагинана в случаях, когда серьезное отравление уже произошло. Для этого мышам из обеих групп сначала вводили смертельную дозу токсичного четыреххлористого углерода, а спустя некоторое время экспериментальной группе — наночастицы селена в каррагинановой оболочке. Мыши из контрольной группы снова не пережили эксперимент, тогда как во второй группе многие выжили. Выживаемость животных была более низкой, чем в профилактическом опыте. Это обусловлено тем, что изначальное отравление оказалось очень мощным. Тем не менее эффект лечения оказался существенным.
До внедрения нового гепатопротектора в медицинскую практику еще далеко. Для начала необходимо закончить всю доклинику. Показать требуемые терапевтические эффекты биологической активности, посмотреть, как препарат будет нейтрализовать другие опасные вещества. «Часть из этих работ уже сделана. Так, в сотрудничестве с Восточно-Сибирским институтом медико-экологических исследований (Ангарск) и Институтом геохимии им. А.П. Виноградова СО РАН (Иркутск) мы установили острую токсичность и некоторые другие токсикологические параметры (результаты этой работы опубликованы в IET Nanobiotechnology). Сейчас совместно с ВСИМЭИ проводится полный комплекс детализированных исследований, направленных на выяснение отсроченной токсичности, а также особенностей воздействия селеновых нанокомпозитов на головной мозг, — объясняет Борис Сухов. — Если в доклинических испытаниях на экспериментальных животных мы не выявим серьезных побочных эффектов, можно будет переходить к клиническим исследованиям на добровольцах, подбирать безопасную дозировку, устанавливать параметры клинической фармакокинетики и фармакодинамики препарата и так далее».
Исследователи рассматривали в качестве оболочки для наночастиц селена и другие галактозосодержащие гепатотропные полисахариды. Высокую эффективность в синтезе антиоксидантных люминесцентных нанокомпозитов элементного селена показали также высокодоступные арабиногалактан лиственницы сибирской 10.1007/s11172-019-2694-x и галактоманнан 10.1007/s11172-020-2988-z.
Ученые ИрИХ СО РАН и ИГХ СО РАН установили также, что новая гепатопротекторная наноселеновая субстанция способна возбуждать и испускать люминесценцию в области прозрачности биотканей. Статья об этом опубликована в журнале Journal of Luminescence. «Это может стать очень хорошим подспорьем для прямой визуальной диагностики как уже описанного антирадикального гепатопротекторного действия наноселена, так и влияния нанокомпозитов селена на другие разнообразные биопроцессы. Но самое главное — у нас открываются принципиально новые возможности для одновременного сочетания терапии и диагностики, то есть тераностики заболеваний», — отмечает Борис Сухов.
Диана Хомякова
Фото Юлии Поздняковой
Информация и фото предоставлены Управлением по пропаганде и популяризации научных достижений СО РАН