Ученые МГУ имени М.В. Ломоносова создали метод маркировки работающих генов, основываясь на различиях активных и неактивных участков хромосом во время репликации из ДНК. Статья опубликована в высокорейтинговом журнале Current Biology.
Ученые МГУ совместно со своими коллегами из США исследовали способы упаковки ДНК в клеточном ядре и их изменение в процессе ее репликативного синтеза. Считается, что характер упаковки ДНК оказывает существенное влияние на работу генов и является одним из механизмов эпигенетического контроля генной экспрессии.
«Эпигенетический контроль генной экспрессии выражается в том, что, хотя все клетки организма имеют одинаковую генетическую информацию, не все гены работают в данном отдельно взятом типе клеток. Именно набор работающих генов определяет судьбу клетки. Существуют несколько клеточных механизмов, которые помогают клетке запомнить, какие гены должны в ней работать, а какие — нет. Это и есть эпигенетический контроль, представляющий собой память клетки о том, кто она и благодаря работе каких генов она такой является, — рассказывает один из авторов статьи, заведующий отделом электронной микроскопии НИИ физико-химической биологии имени А.Н. Белозерского, доктор биологических наук Игорь Киреев. — Нас интересовали так называемые высшие уровни структурной организации хромосом, формирующиеся в результате серии последовательных этапов упаковки нити ДНК».
ДНК в клетке существует в виде комплекса с белками — хроматина. Начальные этапы компактизации хроматина достаточно хорошо исследованы — это нуклеосомы, белковые глобулы размером около 10 нм, состоящие из восьми молекул белков-гистонов, на которые наматывается ДНК. Затем цепочка нуклеосом укладывается непонятным пока образом в более толстые фибриллы, хромонемы, в результате чего достигается очень высокая степень компактизации. Так, длина максимально компактизованной митотической хромосомы в 20 000 раз меньше длины уложенной в ней ДНК.
Репликация — это процесс синтеза дочерней молекулы ДНК на матрице родительской молекулы, а транскрипция — процесс синтеза РНК с использованием ДНК в качестве матрицы. ДНК в составе хромосом чрезвычайно плотно и сложно упакована, и традиционно считалось, что для осуществления процессов матричного синтеза (транскрипция и репликация) эта упаковка мешает и должна быть нарушена в масштабе довольно больших по размеру хроматиновых доменов. Идентифицировать эти домены и проанализировать их структурную организацию с высоким пространственным разрешением, не нарушив при этом их естественной структуры, было достаточно сложно.
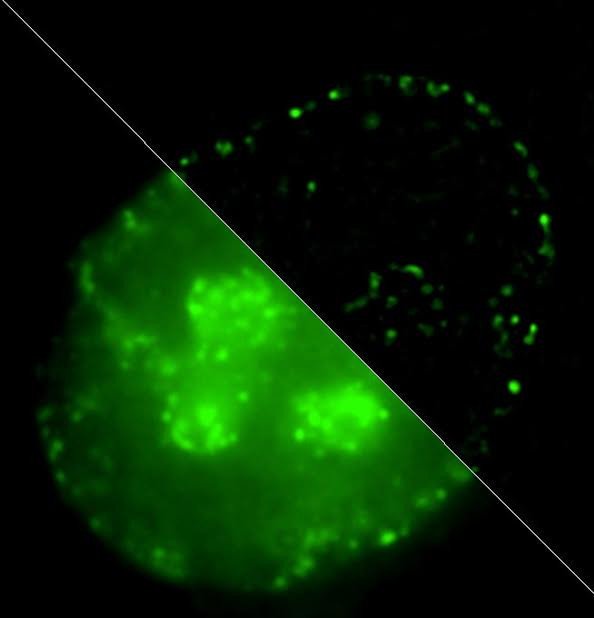
«Мы предложили метод маркировки работающих генов, основываясь на различиях активных и неактивных хромосомных участков во времени репликации из ДНК. Так, активно работающий участок, так называемый эухроматин, реплицируется в самом начале синтетического периода клеточного цикла, а «молчащий» — гетерохроматин — во второй его половине, — комментирует Игорь Киреев. — Наш метод позволил осуществлять недеструктивные (неразрушающие) исследования хроматина. Он основан на комбинации мечения новосинтезированной (дочерней) ДНК методами click-химии с последующей детекций продуктов реакции методами корреляционной флуоресцентной микроскопии с суперразрешением и иммуноэлектронной микроскопии. Иными словами, одну и ту же молекулу в данной клетке мы можем видеть и в оптический, и в электронный микроскоп».
Используя данный подход, ученые сделали два неожиданных наблюдения. Во-первых, «работающий» хроматин, вопреки традиционным представлениям, сохраняет весьма высокую степень упаковки, поскольку он представлен высоко структурированными хроматиновыми фибриллами высшего порядка — хромонемами. Во-вторых, оказалось, что ДНК в составе хромонем обладает высокой структурной пластичностью, то есть способна как бы «перетекать» из одного участка хромонемы в соседний. При этом общая плотная структура хромонемы не изменяется. Эти наблюдения не укладываются в рамки существующих теорий о пространственной организации хромосом, но в то же время позволяют высказать новые гипотезы о механизмах передачи эпигенетической информации в процессе клеточного деления.
«Мы сделали предположение о том, что в новой дочерней клетке структуры хроматина могут перемещаться внутри неё, а не являться фиксированными, взаимодействуя с той ДНК, которая ещё не удваивалась и «помнит всё», а также содержит необходимые молекулярные компоненты для восстановления утраченной эпигенетической информации», — продолжает Игорь Киреев.
Другой вывод, озвученный в статье, опубликованной в Current Biology, состоит в том, что структурная организация генома не является жесткой иерархией. Конечно, есть некие последовательные уровни организации ДНК. Раньше думали, что должна быть четко зафиксированная система, которая однозначно приводит к формированию хромосом. Сейчас оказывается, что всё может быть по-другому: есть некие принципы построения, но внутри заданных границ ДНК обладает некоторой свободой и пластичностью.
«Дальнейшее развитие исследований состоит, во-первых, в переходе к анализу индивидуальных хромосомных локусов, которые мы планируем маркировать (выделять) на оптическом и электронно-микроскопическом уровнях при помощи технологии TALE, а во-вторых, в разработке еще более нативных методов in vivo мечения, совместимых с такими передовыми технологиями, как криоэлектронная микроскопия», — делится планами на будущее Игорь Киреев.
Ученые надеются вплотную приблизиться к расшифровке принципов пространственной организации ДНК, используя прямые методы анализа при помощи визуализации способов упаковки хроматина с высоким разрешением. В практическом плане исследования позволят выяснить структурные аспекты эпигенетического контроля генной экспрессии и, возможно, подсказать пути его регулирования, что позволит разрабатывать более эффективные подходы для терапевтических воздействий, например, при борьбе с раком и старением — состояниями, в которых очень ярко выражена «эпигенетическая» компонента.